
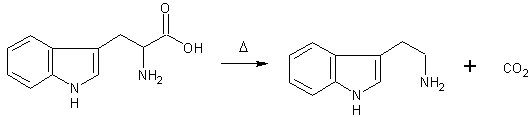
102,1 г L- или DL-триптофана (0,5 моля) суспендируют в 250 мл тетралина содержащего 4,3 г (00,05 моля) 3-пентанона и смесь кипятят с обратным холодильником 8-10 часов с интенсивным перемешиванием до прекращения выделения углекислого газа (4 часа). После этого растворитель удаляют под вакуумом на роторном испарителе. Остаток перегоняют в вакууме получая желтый кристаллический продукт, т. кип 140-155/0,25 торр (лит. 137/0,15 торр), который кристаллизуют из кипящего бензола получая желтые призмы с т.пл. 116-117,5 С (лит. 115-117 С). Выход 67,1 г (83,9%).
В качестве катализатора могут быть использованы и другие карбонильные соединения (в скобках выход): ацетон (75%), 2-бутанон (84,4%), 2-пентанон (86,2%), ацетилацетон (68,7%), 4-оксопентановая кислота (51,2%), циклогексанон (75,0%), бензальдегид (56,9%), 2-гидроксибензальдегид (66,9%), фурфурол (58,1%), ацетофенон (68,7%), бензофенон (79,0%), бензоин (67,5%).

К суспензии 12,25 ммоля DL-триптофана в 30 мл уайт-спирита добавили 25 ммоля L-карвона под потоком азота. Смесь кипятили с обратным холодильником до получения прозрачного раствора и отсутствия триптофана по ТСХ (хлороформ - метанол - раствор аммиака, 9:1:0,1 по объему). Для извлечения продукта использовалась кислотно-основная экстракция 10% соляной кислотой (30 мл). Затем добавили 10% раствор гидроксида натрия до щелочной реакции среды и свободное основание экстрагировали дважды по 30 мл хлороформа. Хлороформенный экстракт упарили получив триптамин с выходом 95%. В качестве примеси в реакции из катализатора получается карболин. Продукты характеризовали ГХ/Мс.
В реакции возможно использование других растворителей и катализаторов, но выход при этом меньше. Были использованы следующие пары растворитель - катализатор (в скобках указан выход триптамина): 1-гексанол + масло мяты курчавой (90%), уайт-спирт + масло мяты перечной (75%), уайт-спирт + 2-бутанон (75%), уайт-спирт + D-пулегон (71%), уайт-спирт + масло мяты курчавой (70%), 1-гексанол + D-пулегон (62%), 1-гексанол + масло мяты болотной (61%), скипидар + D-пулегон (60%), уайт-спирит + ацетон (24%), 2-бутанон без катализатора (20%), ацетон без катализатора (10%).
7,8 г (0,041 моля) 3-(2-нитроэтил)индола в 150 мл 95% этанола смешали с 0,45 г оксида платины и перемешивали с водородом при давлении 41 psi в аппарате для гидрирования при низком давлении до прекращения изменения давления. Катализатор отфильтровали, этанол упарили при пониженном давлении. Светло-коричневый остаток кристаллизовали при охлаждении в бане со льдом, затем растворили в эфире и раствор отфильтровали. К фильтрату добавили ледяную уксусную кислоту до полного осаждения осадка. Осадок ацетата триптамина растворили в воде и подщелочили 2 н. раствором гидроксида натрия. Выпавший триптамин отфильтровали, промыли водой, растворили в бензоле и раствор высушили сульфатом натрия. Часть бензола была упарена в атмосфере азота, охлаждение концентрированного раствора ведет к образованию светло-коричневых кристаллов триптамина (5,1 г, 0,032 моля, 78%) с т.пл. 115-117 С.
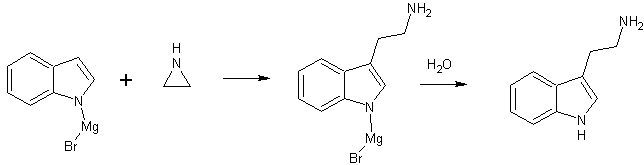
К эфирному раствору 15,6 г (0,13 мол) метилмагнийбромида приливают 15,3 г (0,13 мол) индола в том же растворителе, затем 5,6 г этиленимина в безводном ксилоле. Эфир отгоняют полностью, заменяя его ксилолом, в полученный ксилольный раствор кипятят до затвердения. Разлагают на холоде водой, подкисляет концентрированной соляной кислотой до рН 1 и выделяют хлоргидрат триптамина. Хлоргидрат обрабатывают водным раствором щелочи и получают свободное оонование.
Выход 9,6 г (46%), т.пл. 116°.
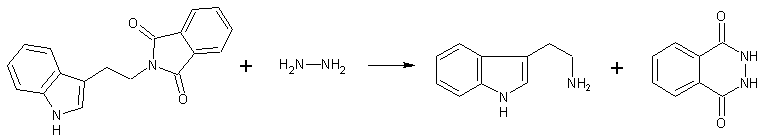
Суспензию 0,02 моль 3-(2-фталимидоэтил)индола в 50 мл метанола нагревают до кипения и прибавляют раствор 1,5 мл (0,03 моль) гидразингидрата в 5 мл метанола. Полученную смесь кипятят 2 часа, метанол отгоняют в вакууме досуха, к остатку приливают 100 мл 2 н. раствора едкого натра и извлекают хлористым метиленом (3 х 350 мл). Экстракт фильтруют и к остатку добавляют абсолютный бензол и снова упаривают досуха. Для очистки триптамина переводят в гидрохлорид, который растворяют в воде и кипятят с активированным углем. После подщелачивания 2 н растором едкого натра продукт извлекают хлористым метиленом.
Выход 94%, т.пл. 114-116 С (из бензола), т.пл. гидрохлорида 248-250 С.
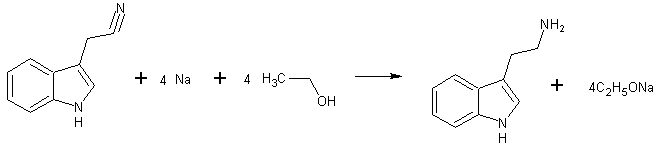
В 100 мл абсолютного спирта растворяют 5 г 3-индолилацетонитрила и нагревают до кипения на водяной бане. В кипящий раствор вносят небольшими кусочками в течение 15 мин 6 г металлического натрия. После тoгo как весь натрий растворится, добавляют 100 мл воды и раствор упаривают до небольшого объема в вакууме (нужно, чтобы отогналась большая часть спирта). Остаток экстрагируют многократно эфиром. Эфирный раствор, который содержит триптамин и нейтральные примеси, обрабатывают 2 н. НСl, тремя порциями по 50 мл. При этом триптамин переходит в солянокислый раствор. Этот раствор подщелачивают избытком едкого натра и вновь извлекают эфиром. Эфирный раствор сушат и эфир отгоняют, в остатке триптамин.
Выход 3-3,5 г (около 65 % от теоретического). Продукт перекристаллизовывают из лигроина. Т. пл. 114,5-115,5°.
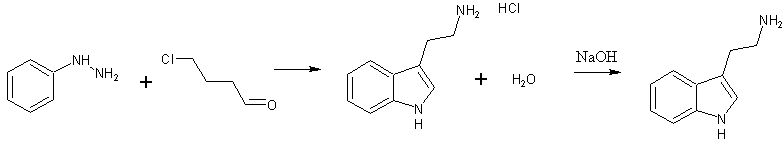
В полулитровой круглодонной колбе, снабженной мощным обратным холодильником, смешивают растворы 10,8 г (0,1 моля) фенилгидразина в 100 мл 80% этилового спирта и 10,6 г (0,1 моля) свежеприготовленного гамма-хлормаслянного альдегида в 200 мл этилового спирта и кипятят на водяной бане в течение 6 часов. Затем в вакууме водоструйного насоса отгоняют растворитель, сухой остаток гидрохлорида триптамина растворяют в 100 мл 0,1 н раствора соляной кислоты и экстрагируют нейтральные примеси 45 мл эфира (3 раза по 15 мл). Водный слой подщелагивают едким натром и выделившийся триптамин экстрагируют бензолом (3 раза по 30 мл). Бензольный экстракт фильтруют, высушивают над прокаленным сернокислым натрием, отгоняют растворитель в вакууме водоструйного насоса и маслообразный остаток перегоняют в токе сухого азота, собирая фракцию, кипящую при 185-188° (0,5 мм.рт.ст.). Полученное желтоватое густое масло быстро затвердевает. При необходимости перекристаллизовывают из 50 мл смеси петролейного эфира и бензола 3:1.
Выход 11,2 г (70,0% от теоретического).
С кислотами образует соли.