Главная страница
 Базы данных
Базы данных
 База данных свойств веществ (поиск)
База данных свойств веществ (поиск)
Свойства вещества:
фенантрен
Синонимы и иностранные названия:
phenanthrene (англ.)
Тип вещества:
органическое
Внешний вид:
бесцветн. моноклинные кристаллы (растворитель перекристаллизации - этанол)Брутто-формула (по системе Хилла для органических веществ):
C14H10Молекулярная масса (в а.е.м.): 178,24
CAS №: 85-01-8
Температура плавления (в °C):
101Температура кипения (в °C):
340,1Растворимость (в г/100 г растворителя или характеристика):
ацетон: 25,5 (0°C) [Лит.]
ацетон: 51,94 (20°C) [Лит.]
бензин: 4,53 (15,5°C) [Лит.]
бензин: 6,3 (30°C) [Лит.]
бензол: 29,86 (5°C) [Лит.]
бензол: 51,7 (20°C) [Лит.]
бензол: 69,68 (30°C) [Лит.]
валериановая кислота: 19,9 (39°C) [Лит.]
вода: 0,0001 (25°C) [Лит.]
вода: 0,000148 (30,3°C) [Лит.]
вода: 0,0001845 (34,53°C) [Лит.]
вода: 0,00152 (73,4°C) [Лит.]
гексан: 9,15 (25°C) [Лит.]
диоксид серы: 29,9 (20°C) [Лит.]
диэтиловый эфир: 8,93 (15°C) [Лит.]
изомасляная кислота: 14 (23°C) [Лит.]
масляная кислота: 18,5 (23°C) [Лит.]
масляная кислота: 26,6 (39°C) [Лит.]
метанол: 1,2 (0°C) [Лит.]
метанол: 3,18 (20°C) [Лит.]
метанол: 4,8 (30°C) [Лит.]
метиламин: легко растворим [Лит.]
муравьиная кислота 95%: 0,46 (20,8°C) [Лит.]
пропионовая кислота: 20,5 (23°C) [Лит.]
сероуглерод: 45,88 (5°C) [Лит.]
сероуглерод: 72,08 (20°C) [Лит.]
сероуглерод: 89,82 (30°C) [Лит.]
тетрахлорметан: 7,6 (0°C) [Лит.]
тетрахлорметан: 12,66 (10°C) [Лит.]
тетрахлорметан: 19 (20°C) [Лит.]
тетрахлорметан: 26,2 (30°C) [Лит.]
толуол: 13,8 (15,5°C) [Лит.]
уксусная кислота: 9,06 (23°C) [Лит.]
хлороформ: 25,5 (0°C) [Лит.]
хлороформ: 46,6 (20°C) [Лит.]
хлороформ: 64,2 (30°C) [Лит.]
циклогексан: 7,18 (20,7°C) [Лит.]
этанол: 2 (14°C) [Лит.]
этанол: 4,91 (25°C) [Лит.]
этанол: 10 (78°C) [Лит.]
этанол абсолютный: 4,15 (20°C) [Лит.]
Плотность:
0,98 (4°C, г/см3, состояние вещества - кристаллы)
1,063 (100°C, г/см3, состояние вещества - кристаллы)
Нормативные документы, связанные с веществом:
- МУК № 4.1.1044-01 "Хромато-масс-спектрометрическое определение полициклических ароматических углеводородов в воздухе" (Описание документа: Концентрирование на адсорбент, экстракция эфиром, упаривание, реэкстракция хлороформом, ГЖХ/МС на капиллярной колонке.)
- МУК № 4.1.1062-01 "Хромато-масс-спектрометрическое определение труднолетучих органических веществ в почве и отходах производства и потребления"
- ПНД В МСУ Хж № 3.4-018-04 "Методика выполнения измерений массовых концентраций полициклических ароматических углеводородов в пробах сточных, очищенных сточных и природных вод методом высокоэффективной жидкостной хроматографии с флуориметрическим детектированием" (Описание документа: Экстракция из воды гексаном, концентрирование, очистка экстракта и ВЭЖХ анализ с градиентным элюированием и флуориметрическим детектированием.)
- ПНД В МСУ Хж № 5.6-024-06 "Методика выполнения измерений массовых концентраций полициклических ароматических углеводородов в пробах почвы и донных отложений методом высокоэффективной жидкостной хроматографии" (Описание документа: Экстракция ПАУ ацетоном, реэкстракция гексаном, очистка экстракта, концентрирование и ВЭЖХ анализ с градиентным элюированием и флуориметрическим детектированием.)
- ПНД Ф № 14.1:2:4.70-96 издание 2004 г "Методика выполнения измерений массовой концентрации полициклических ароматических углеводородов в пробах питьевых, природных и сточных вод хроматографическим методом ВЭЖХ" (Описание документа: Анализ вод методом ВЭЖХ после экстракции гексаном.)
Способы получения:
- Декарбоксилированием фенантрен-9-карбоновой кислоты. (выход 64%) [Лит.]
- Облучение смеси транс-стильбена с иодом в циклогексане светом ртутной лампы в присутствии кислорода дает чистый фенантрен. Выход 73%. [Лит.1]
- Из 9-флуоренилкарбинола под действием пентаоксида фосфора образуется фенантрен. Выход 100%. [Лит.1]
Реакции вещества:
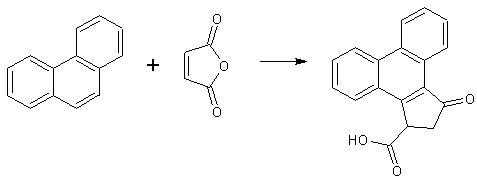
- Реагирует с малеиновым ангидридом в нитробензоле в присутствии хлорида алюминия с образованием оксоциклопентафенантренкарбоновой кислоты. [Лит.]
- Гидрируется водородом при 130 С и давлении 203 атм на катализаторе Адкинса (смесь оксидов хрома и меди) до 9,10-дигидрофенантрена. (выход 70%) [Лит.]
Показатель преломления (для D-линии натрия):
1,5943 (20°C)
Индекс удерживания для газовой хроматографии:
1789,2 (фаза колонки - DB-5, со скоростью подъема температуры 6 К/мин)
Дипольный момент молекулы (в дебаях):
0 (20°C)
Удельная теплоемкость при постоянном давлении (в Дж/г·K):
1,159 (10°C)
Энтальпия кипения ΔHкип (кДж/моль):
52,97Теплота сгорания (кДж/моль):
7081,4Летальная доза (ЛД50, в мг/кг):
1800-2000 (крысы, внутрижелудочно)
Биологическое действие:
Растения. Угнетает рост и развитие растений свеклы. Кончики корешков свеклы чернеют и отмирают на 3-4 сутки воздействия фенантрена.
Животные. Не обладает канцерогенными свойствами в опытах на животных.
Дополнительная информация::
Реагирует с хлором или бромом с образованием 9,10-дигалогенфенантренов. Нитрование фенантрена смесью азотной, уксусной кислот и уксусного ангидрида приводит к смеси 9- (наиболее количество), 1- и 3-нитрофенантренов. Легко сульфируется.
Действием натрия в амиловом спирте восстанавливается до смеси 1,2,3,4-тетрагидрофенантрена (тетрантрена) и 9,10-дигидрофенантрена.
Источники информации:
- Seidell A. Solubilities of organic compounds. - 3ed., vol.2. - New York: D. Van Nostrand Company, 1941. - С. 742-744
- Yalkowsky S.H., Yan H. Handbook of aqueous solubility data. - CRC Press, 2003. - С. 948-948
- Yalkowsky S.H., Yan H., Jain P. Handbook of aqueous solubility data. – 2nd ed. - CRC Press, 2010. - С. 989-991
- Вредные вещества в промышленности: Справочник для химиков, инженеров и врачей. - 7-е изд., Т.1. - Л.: Химия, 1976. - С. 136-137
- Другов Ю.С., Родин А.А. Мониторинг органических загрязнений природной среды. - СПб.: Наука, 2004. - С. 129, 708
- Клар Э. Полициклические углеводороды. - Т.1. - М.: Химия, 1971. - С. 220-232
- Рабинович В.А., Хавин З.Я. Краткий химический справочник. - Л.: Химия, 1977. - С. 187
- Справочник по растворимости. - Т.1, Кн.2. - М.-Л.: ИАН СССР, 1962. - С. 975, 1036-1037, 1049-1050, 1095, 1114, 1148, 1193-1194, 1242, 1281, 1348, 1441, 1465, 1564-1565 (растворимость в органических растворителях)
- Токсикологический вестник. - 2001. - №5. - С. 35-36
- Химическая энциклопедия. - Т. 5. - М.: Советская энциклопедия, 1999. - С. 62-63
Если не нашли нужное вещество или свойства можно выполнить следующие действия:
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Руслан Анатольевич Кипер