
Трубку из пирекса длиной 600 мм и диаметром 25 мм промывают горячей азотной кислотой, ополаскивают водой и выдерживают при 450° в течение 2 час. с одновременным пропусканием медленного тока азота.
Смесь 20,0 г (0,253 мол.) селена и 100 г окиси алюминия в гранулах диаметром 1—3 мм помещают в очищенную трубку, которую в свою очередь укрепляют в печи (примечание 1). Смесь нагревают в токе азота; по достижении 450° (примечание 2) азот заменяют ацетиленом. Через несколько минут газ в трубке вспыхивает, отлагая углистый налёт на катализаторе и стенках. Если вспышки не происходит, то шлиф, через который вводится ацетилен, на одну секунду отсоединяют, что позволяет небольшому количеству воздуха попасть внутрь.
Реакция продолжается 7—8 час. и после этого замедляется настолько, что вести дальнейший синтез уже невыгодно.
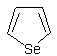
Сырой продукт, собранный в ходе нескольких таких синтезов, объединяют и перегоняют, собирая фракцию с т. кип. 105—120°. Продукт содержит 95% селенофена, что удовлетворительно для большинства синтезов (примечание 3).
Извлечённый из охладившейся реакционной трубки катализатор (примечание 4) представляет собой окись алюминия, покрытую чёрным налётом. Он может быть успешно применён 25 раз без заметного падения эффективности (примечание 5).
Примечания
1. Синтез можно проводить в нескольких трубках одновременно. Авторы рекомендуют применять десять трубок, что позволяет обрабатывать за раз 200 г селена и производить 150—200 г селенофена в день.
2. Образование селенофена при температуре менее 340° протекает чрезвычайно медленно, а при повышении её до 550° образование примесных углеводородов становится заметным даже с носителем. Приведённые условия дают наилучший выход.
3. Продукт, получаемый пропусканием ацетилена над чистым селеном, состоит в основном из бензола и толуола. Он содержит лишь около 5% селенофена, который трудно отделяется от толуола (т. кип. 110°), и 10% высококипящих веществ. В прошлых работах на факт присутствия толуола не обращали достаточного внимания. Употребление окиси алюминия снижает содержание бензола и толуола в сыром продукте до 2—3%.
4. Окись алюминия легко отравляется парами концентрированной азотной кислоты и, при обычной температуре, газообразными побочными продуктами настоящего синтеза, вероятнее всего селенистым водородом. Трубка с катализатором, хранившаяся в том же вытяжном шкафу, что и печь, дала селенофен с выходом менее 5%.
5. Свежий катализатор даёт меньше селенофена, чем использованный повторно. В ходе первых пяти-шести циклов выход постепенно возрастает от 5 до 50%, а при последующих колеблется от 50 до 70%. Средний выход перегнанного селенофена, получаемого на старом катализаторе, составляет 58% по селену.
(Пер. с англ. Bitrex)
В сравнительно мягких условиях мало чувствителен к действию кислот, щелочей, а также окислителей и восстановителей.