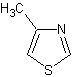

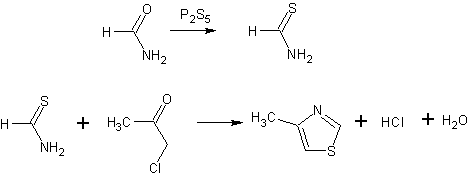
В литровую трехгорлую колбу, снабженную обратным холодильником, капельной воронкой и мощной мешалкой (примечание 1), помещают 60 г (0,27 моля) порошкообразного пятисернистого фосфора, 260 мл бензола (примечание 2) и 60 мл (1,5 моля) формамида. В капельную воронку помещают раствор 81 мл (1 моль) хлорацетона (примечание 3) и 50 мл бензола и 3—5 мл этого раствора при перемешивании приливают в реакционную колбу.
Реакция начинается при слабом нагревании колбы па закрытой электрической плитке. Далее ее умеренное течение поддерживают регулированием притока раствора хлорацетона в продолжение 1,5-2 часов без нагревания. По окончании прибавления, не переставая перемешивать, кипятят 2—3 часа и после охлаждения к темно-коричневой реакционной смеси приливают 200 мл воды. Хорошо перемешивают, отделяют бензольный слой (примечание 4) и экстрагируют его два раза 2N соляной кислотой, порциями по 50 мл. Соединенные полные экстракты хлоргидрата осторожно подщелачивают 150 г едкого кали (примечание 5) и экстрагируют эфиром; сначала 200 мл, а затем 3 раза по 100 мл. Эфирный раствор высушивают над едким кали (примечание 6) и фильтруют. Растворитель отгоняют из колбы, снабженной высокой колонкой, а остаток перегоняют при атмосферном давлении, собирая фракцию, кипящую при 130—135°С; n = 1,5195—1,5205 (примечание 7).
Выход 55,5—61,8 г, или 56,0—62,3% теоретического количества (примечание 8).
Примечания
1. Опыт проводят в хорошо действующем вытяжном шкафу. Ввиду нерастворимости хлоргидрата в бензоле образуется вязкая масса, задерживающая движение мешалки.
2. В реакции использован бензол, не содержащий тиофена. Применение технического бензола снижает выход до 30% теоретического количества.
3. Были применены продажные химически чистые пятисернистый фосфор, формамид н технический хлорацетон. Повторно перегнанный хлорацетон не повышает выход. Большой избыток пятисернистого фосфора вызывает образование смолистых веществ, снижающих выход.
4. При добавлении воды образуется мелкий темно-коричневый осадок. Выделение органического слоя можно облегчить фильтрацией реакционной смеси, однако этот процесс протекает очень медленно.
5. Едкое кали в гранулах удобнее добавлять через обратный холодильник, присоединенный к делительной воронке. В случае применения едкого натра при охлаждении выделяется большой избыток неорганического вещества (очевидно фосфат натрия), который затрудняет экстракцию.
6. На гранулах едкого кали может осаждаться слой полимера.
7. Во избежание разложения к концу перегонки применяют слегка пониженное давление. Эта фракция достаточно чиста для последующих реакций. При повторной перегонке получается чистый 4-метилтиазол с т. кип. 133,5—134,5 С и n = 1,5200, однако процесс сопровождается потерями в пределах до 6%.
8. Из головной фракции с т. кип. 40—130°, при повторной перегонке, выделяется еще 1,5—2 г вещества. В случае использования 0,5 моля хлорацетона выход 4-метилтиазола составляет около 62%. Увеличение количества исходного продукта до 2 молей, ввиду трудности перемешивания реакционной массы, снижает выход.